2012年,首個基因治療藥物Glybera獲歐盟批準(zhǔn),該藥物基于腺相關(guān)病毒(AAV)載體用于家族性脂蛋白脂酶缺乏(LPLD)成人患者的治療。
去年,F(xiàn)DA批準(zhǔn)的第一個體內(nèi)基因療法是Luxturna,同樣使用AAV作為遞送載體,它被施用于眼睛以治療罕見的遺傳性失明。

1965年,AAV首次被發(fā)現(xiàn)為腺病毒樣本的污染物。但許多病毒學(xué)家認為研究它們是浪費時間,因為它們不會引發(fā)任何疾病,而這一事實后來成為基因治療的最大資產(chǎn)(使其不太可能引起極端的免疫反應(yīng))。在當(dāng)時過去的35年里,科學(xué)家們只發(fā)現(xiàn)了六種AAV變體,盡管它們看起來很安全,但沒有一種特別擅長遞送基因。
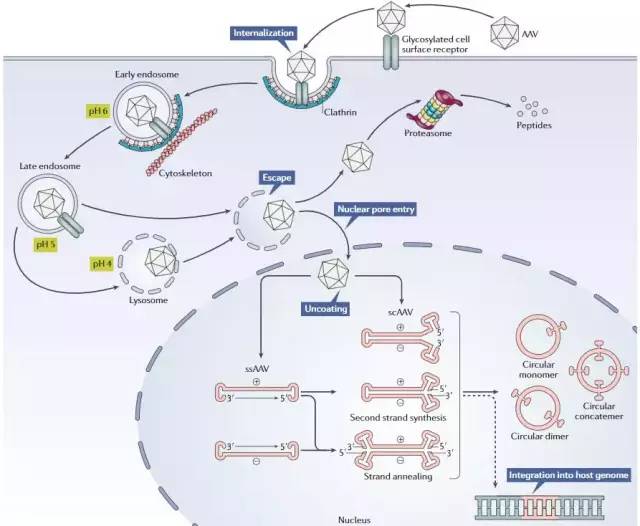
▲ rAAV轉(zhuǎn)導(dǎo)通路(圖片來源:Nature Reviews Drug Discovery)
在純科學(xué)的好奇心驅(qū)使下,一些研究小組開始了解基本AAV生物學(xué)的過程,此時并沒有意識到其作為人類基因治療平臺的巨大潛力。在AAV研究的前15-20年中,AAV的幾個重要方面被表征,包括其基因組構(gòu)型和組成、DNA復(fù)制和轉(zhuǎn)錄、感染潛伏期和病毒粒子組裝。這些成果共同促進了野生型AAV2序列成功克隆到質(zhì)粒中,從而實現(xiàn)了基因研究和整個AAV2基因組測序。早期研究提供了使用AAV作為基因傳遞載體的基礎(chǔ)知識。
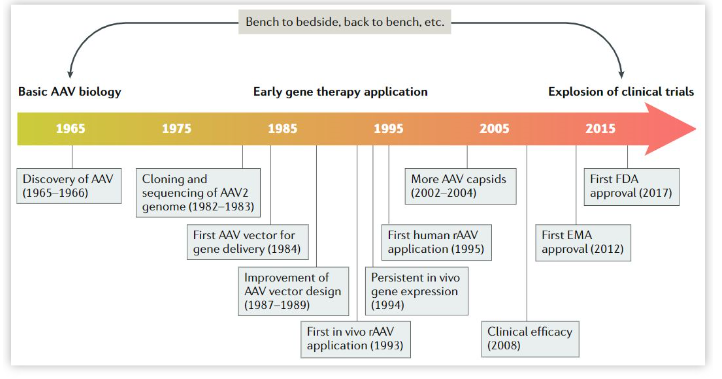
▲50年AAV時間線(圖片來源:Nature Reviews Drug Discovery )
AVV帶來的挑戰(zhàn)
基于安全性和治療性基因容量問題,非病毒遞送方法變得越來越普遍。最簡單的非病毒基因傳遞系統(tǒng)如裸DNA、質(zhì)粒DNA,當(dāng)直接注射到某些組織,特別是肌肉時,可以產(chǎn)生顯著水平的基因表達,但仍然低于用病毒載體實現(xiàn)的基因表達。
目前,病毒載體仍然是基因治療試驗最流行的遞送方法,迄今為止,已用于大約三分之二的試驗。根據(jù)一項2017年的統(tǒng)計,腺病毒是最常用的載體,占所有試驗的20.5%,但自2012年(23.3%)以來有所下降。近年來,逆轉(zhuǎn)錄病毒載體使用率同樣下降(只占試驗的17.4%,而2012年為19.7%,2007年為22.8%,2004年為28%),這很大程度上是由于慢病毒載體(約為7.3%,比2012年的2.9%增加)的出現(xiàn),提高了安全性以及擴大了使用范圍。類似的趨勢發(fā)生在腺相關(guān)病毒(AAV)的使用情況,從2012年的4.9%增加到2017年的7.6%。
可負擔(dān)性已經(jīng)成為了基于病毒的基因療法的主要障礙之一
藥物產(chǎn)品的可負擔(dān)性已經(jīng)成為了基于病毒的基因療法的主要障礙之一。根據(jù)美國知名處方藥比價網(wǎng)站GoodRx發(fā)布的2019年全球最昂貴藥物榜單,兩款A(yù)AV基因療法占據(jù)了前兩名,分別是212.5萬美元的Zolgensma和85萬美元的Luxturna。今年6月,歐盟批準(zhǔn)了Bluebird bio針對重型β地中海貧血的基因療法Zynteglo(LentiGlobin),其使用慢病毒載體轉(zhuǎn)導(dǎo)CD34+細胞,177萬美元的定價使其成為目前全球第二昂貴的藥物。
價格主要歸因于制造的高成本。要想生產(chǎn)足夠的載體用于治療,需要大量的資源和專業(yè)知識以及合適的生產(chǎn)系統(tǒng)。
治療所需的高劑量也帶來了人們對安全性的擔(dān)憂
威爾遜承認,科學(xué)家們?nèi)匀徊煌耆斫鉃槭裁碅AV在一定劑量下會變得有毒,但很明顯,如果沒有更有效的基因遞送工具,高劑量的AAV可能是糾正某些疾病的唯一方法,尤其是肌肉疾病。高劑量還造成了額外的制造障礙和高成本。
這些擔(dān)憂指導(dǎo)了威爾遜的新公司Passage Bio的戰(zhàn)略,該公司專注于研究罕見的遺傳神經(jīng)疾病。該公司臨時首席執(zhí)行官奧比米德?斯奎托(OrbiMed's Squinto)表示:“我們一直在努力選擇需要非常、非常低劑量治療的疾病。”該公司還計劃將AAVs直接注射到腦脊液中,這應(yīng)該比Zolgensma使用的全身注射需要更小的劑量。斯奎托說:“威爾遜在他的職業(yè)生涯中不會再冒太多的風(fēng)險了。在進行人體實驗之前,我們將盡可能地了解更多。”
免疫障礙同樣存在于當(dāng)前基因療法的開發(fā)過程中
例如,重組AAV蛋白衣殼、其基因組和轉(zhuǎn)基因的蛋白質(zhì)產(chǎn)物可以在多個階段與宿主免疫系統(tǒng)相互作用,對有效基因遞送和持久基因表達構(gòu)成障礙。目前,中和抗體(Nab)篩查和排除血清反應(yīng)陽性受試者仍然是許多臨床研究中的必要步驟。
解決策略
為了避免免疫應(yīng)答可能導(dǎo)致的問題,研究人員正在測試各種策略,以最小化基因治療帶來的免疫應(yīng)答。例如,針對免疫特權(quán)部位(如眼睛和大腦)的疾病開發(fā)基因療法,一來規(guī)避免疫應(yīng)答帶來的風(fēng)險,二來只需少量施用載體,也避免了臨床應(yīng)用的制造問題。
目前,在遺傳性視網(wǎng)膜疾病和中樞神經(jīng)系統(tǒng)疾病的臨床試驗中,AAV已經(jīng)實現(xiàn)了相對的安全性和耐受性。另外,還有證據(jù)表明轉(zhuǎn)基因靶向肝臟能誘導(dǎo)免疫耐受。
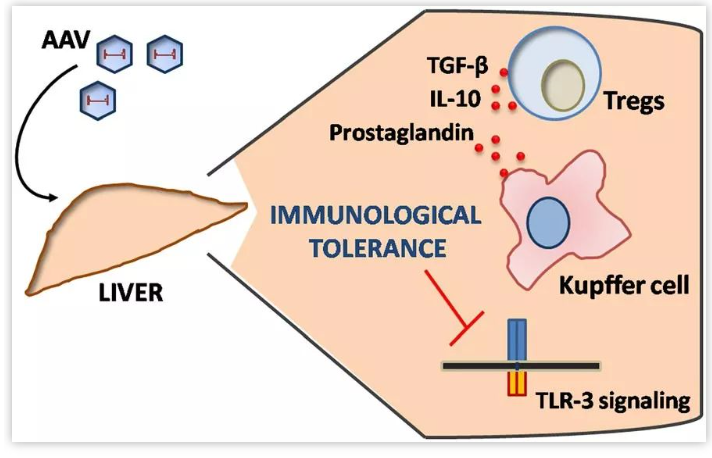
▲AAV介導(dǎo)的基因轉(zhuǎn)移后促成肝臟免疫耐受(圖片來源:annualreviews)
基因治療的安全性得到更多的重視,人們也更加了解可能出現(xiàn)的臨床試驗中可能出現(xiàn)問題,以及擁有相應(yīng)的措施。一般的基因治療,尤其是基于AAV載體的基因治療,已經(jīng)十分成熟。基因療法代表了治愈人類疾病的前沿之一,基因遞送載體的革新極大地推動了該領(lǐng)域的發(fā)展。挑戰(zhàn)仍然存在,使命還遠未達成!
「免疫應(yīng)答」在AAV基因治療中的挑戰(zhàn)與解決策略
基因治療時代人物威爾遜:20年致力于安全病毒載體的研究,他見證了低沉到華麗回歸
華人學(xué)者高光坪Nature子刊發(fā)文,詳述基因治療明星載體腺相關(guān)病毒(AAV)丨醫(yī)麥猛爆料

